Page 171 - Korniy_dyser
P. 171
171
лужне середовище або іони гідроксиду, що пов’язано із найбільшою енергією
–
зв’язку ОН на поверхні алюмінію. Таким чином побудовані залежності
дають можливість оцінювати корозійне розчинення за наявності компонентів
середовища встановленням енергетичних бар’єрів виходу іонів металів.
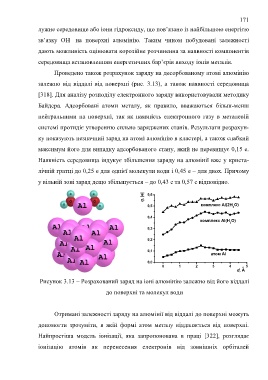
Проведено також розрахунок заряду на десорбованому атомі алюмінію
залежно від віддалі від поверхні (рис. 3.13), а також наявності середовища
[318]. Для аналізу розподілу електронного заряду використовували методику
Байдера. Адсорбовані атоми металу, як правило, вважаються більш-менш
нейтральними на поверхні, так як наявність електронного газу в металевій
системі протидіє утворенню сильно заряджених станів. Результати розрахун-
ку показують незначний заряд на атомі алюмінію в кластері, а також слабкий
максимум його для випадку адсорбованого стану, який не перевищує 0,15 е.
Наявність середовища індукує збільшення заряду на алюмінії вже у криста-
лічній гратці до 0,25 е для однієї молекули води і 0,45 е – для двох. Причому
у вільній зоні заряд дещо збільшується – до 0,43 е та 0,57 е відповідно.
q, |e| 0,6
0,5 комплекс Al(2Н O)
2
0,4
комплекс Al(Н O)
2
0,3
0,2
0,1
атом Al
0,0
0 1 2 3 4 o 5
d, A
Рисунок 3.13 – Розрахований заряд на іоні алюмінію залежно від його віддалі
до поверхні та молекул води
Отримані залежності заряду на алюмінії від віддалі до поверхні можуть
допомогти зрозуміти, в якій формі атом металу віддаляється від поверхні.
Найпростіша модель іонізації, яка запропонована в праці [322], розглядає
іонізацію атомів як перенесення електронів від зовнішніх орбіталей