Page 160 - Дисертація_Влад_Христина_Ігорівна
P. 160
Кінетика електрохімічної реакції водню зазвичай характеризується
густиною струму обміну. На рис. 3.66 подано криві лінійної поляризації. Зразки
з найвищим значенням I свідчать про швидкий перенесення заряду на межі
0
сплав/електроліт. Поляризаційний опір, який у досліджених зразках становить
від 127 до 459 мОм.У багатьох випадках значення I , що перевищують 100
0
мА/г, також пов’язані з високими показниками HRD (див. табл. 3.26).
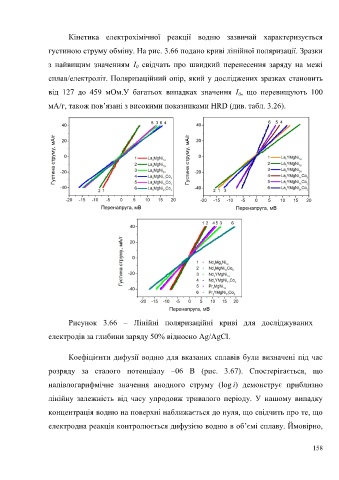
Рисунок 3.66 – Лінійні поляризаційні криві для досліджуваних
електродів за глибини заряду 50% відносно Ag/AgCl.
Коефіцієнти дифузії водню для вказаних сплавів були визначені під час
розряду за сталого потенціалу –06 В (рис. 3.67). Спостерігається, що
напівлогарифмічне значення анодного струму (lоg i) демонструє приблизно
лінійну залежність від часу упродовж тривалого періоду. У нашому випадку
концентрація водню на поверхні наближається до нуля, що свідчить про те, що
електродна реакція контролюється дифузією водню в об’ємі сплаву. Ймовірно,
158