Page 278 - Korniy_dyser
P. 278
278
відповідно). Це говорить про більшу імовірність дисоціації О 2, ніж її
хемосорбційної взаємодії.
E A , Е b , еВ 5.0 Енергія активації
4.5
Енергія з'вязку О
2
4.0 Енергія з'вязку О
3.5
3.0
1.0
0.5
0.0
Pt Pt Co 13 Pt Co 13
42
42
55
пропорційна оболонкова
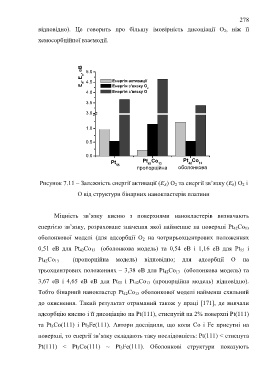
Рисунок 7.11 – Залежність енергії активації (Е А) О 2 та енергії зв’язку (Е b) О 2 і
О від структури бінарних нанокластерів платини
Міцність зв’язку кисню з поверхнями нанокластерів визначають
енергією зв’язку, розраховане значення якої найменше на поверхні Pt 42Co 13
оболонкової моделі (для адсорбції О 2 на чотрирьохцентрових положеннях
0,51 еВ для Pt 42Co 13 (оболонкова модель) та 0,54 еВ і 1,16 еВ для Pt 55 і
Pt 42Co 13 (пропорційна модель) відповідно; для адсорбції О на
трьохцентрових положеннях – 3,38 еВ для Pt 42Co 13 (оболонкова модель) та
3,67 еВ і 4,65 еВ еВ для Pt 55 і Pt 42Co 13 (пропорційна модель) відповідно).
Тобто бінарний нанокластер Pt 42Co 13 оболонкової моделі найменш схильний
до окиснення. Такий результат отриманий також у праці [171], де вивчали
адсорбцію кисню і її дисоціацію на Pt(111), стиснутій на 2% поверхні Pt(111)
та Pt 3Co(111) і Pt 3Fe(111). Автори дослідили, що коли Со і Fe присутні на
поверхні, то енергії зв’язку складають таку послідовність: Pt(111) < стиснута
Pt(111) < Pt 3Co(111) ~ Pt 3Fe(111). Оболонкові структури показують