Page 140 - Korniy_dyser
P. 140
140
квазіоктаедричному оточенні. Зростав позитивний заряд на атомах заліза і
міді, що свідчить про перенос електронів на зону Фермі металу. Виділена
енергія наближалась до теплоти гідратації відповідних аквакомплексів.
Дальший розрахунок показав, що гідратовані іони металу поступово
віддалялись від поверхні металів на 3 Å, виходили у середовище або
залишались на поверхні, втрачаючи гідратну оболонку, а нейтральний заряд
поверхневого атома металу відновлювався. Описане явище відповідає
зворотній електрохімічній реакції.
У момент утворення приповерхневого аквакомплексу металу можна
оцінити його електрохімічний мікропотенціал, знаходячи відношення енергії
гідратації комплексу до його ефективного заряду. Однак отримані абсолютні
значення не можна порівнювати з відносними експериментальними, а тільки
із потенціалами водневого електрода. Тому будували його модель, що
складалась із кластера-підкладки, утвореного атомами платини, на поверхні
(111) якого адсорбувались молекули води та водню. Розглянули дисоціативну
хемосорбцію молекул водню з подальшою іонізацією та гідратацією (рис. 2.
22).
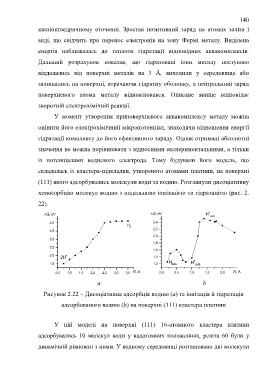
G, eV G, eV H +
sol
4,0 2,4
H
2
3,5 2,2
2,0
3,0
1,8
2,5
1,6
2,0 +
2H 1,4
H +
1,5 1,2 ads H ads
0,5 1,0 1,5 2,0 2,5 3,0 3,5 R, A 0,0 0,5 1,0 1,5 2,0 R, A
а b
Рисунок 2.22 – Дисоціативна адсорбція водню (а) та іонізація й гідратація
адсорбованого водню (b) на поверхні (111) кластера платини
У цій моделі на поверхні (111) 16-атомного кластера платини
адсорбувались 10 молекул води у надатомних положеннях, решта 60 були у
динамічній рівновазі з ними. У водному середовищі розташовано дві молекули