Page 228 - Korniy_dyser
P. 228
228
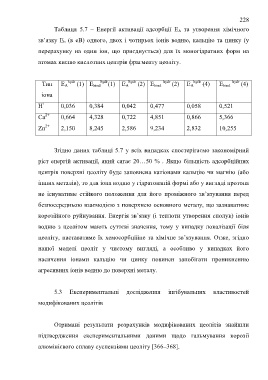
Таблиця 5.7 – Енергії активації адсорбції Е А та утворення хімічного
зв’язку Е b (в еВ) одного, двох і чотирьох іонів водню, кальцію та цинку (у
перерахунку на один іон, що приєднується) для їх моногідратних форм на
атомах кисню кислотних центрів фрагменту цеоліту.
Тип Е А hydr (1) Е bind hydr (1) Е А hydr (2) Е bind hydr (2) Е А hydr (4) Е bind hydr (4)
іона
+
H 0,036 0,384 0,042 0,477 0,058 0,521
2+
Ca 0,664 4,328 0,722 4,851 0,866 5,366
2+
Zn 2,150 8,245 2,586 9,234 2,832 10,255
Згідно даних таблиці 5.7 у всіх випадках спостерігаємо закономірний
ріст енергій активації, який сягає 20…50 % . Якщо більшість адсорбційних
центрів поверхні цеоліту буде заповнена катіонами кальцію чи магнію (або
інших металів), то для іона водню у гідратованій формі або у вигляді протона
не існуватиме стійкого положення для його проміжного зв’язування перед
безпосередньою взаємодією з поверхнею основного металу, що зазнаватиме
корозійного руйнування. Енергія зв’язку (і теплоти утворення сполук) іонів
водню з цеолітом мають суттєві значення, тому у випадку локалізації біля
цеоліту, наставатиме їх хемосорбційне та хімічне зв’язування. Отже, згідно
нашої моделі цеоліт у чистому вигляді, а особливо у випадках його
насичення іонами кальцію чи цинку повинен запобігати проникненню
агресивних іонів водню до поверхні металу.
5.3 Експериментальні дослідження інгібувальних властивостей
модифікованих цеолітів
Отримані результати розрахунків модифікованих цеолітів знайшли
підтвердження експериментальними даними щодо гальмування корозії
алюмінієвого сплаву суспензіями цеоліту [366–368].