Page 18 - Microsoft Word - aref_Korniy_final.doc
P. 18
16
Для підтвердження експериментальних
результатів вивчали особливості електронної і
геометричної структур молекул рамноліпіду та
енергетику їх взаємодії з катіонами алюмінію,
міді, цинку та кальцію, які зв’язуються з
певними адсорбційними центрами молекули.
Результати квантово-хімічного розрахунку
свідчать, що електронні та геометричні
характеристики молекули рамноліпіду
(молекулярна формула – C 26H 48O 9) є важливи-
ми параметрами для прогнозування її реакцій-
ної здатності на поверхні металу. Зокрема,
гідрофобні ланцюги (–СН 2–) n–СН 3 у молекулі
та кільце орієнтовані в різних площинах, що
може суттєво впливати на формування зв’язків
рамноліпіду з поверхнею металу (рис. 11).
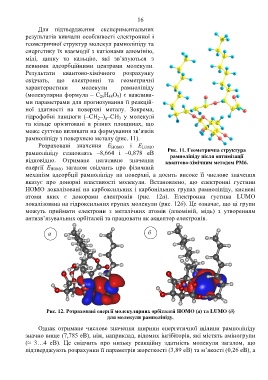
Розраховані значення E HOMO і E LUMO
Рис. 11. Геометрична структура
рамноліпіду становлять –8,664 і –0,878 еВ
рамноліпіду після оптимізації
відповідно. Отримане негативне значення квантово-хімічним методом PM6.
енергії Е HOMO загалом свідчить про фізичний
механізм адсорбції рамноліпіду на поверхні, а досить високе її числове значення
вказує про донорні властивості молекули. Встановлено, що електронні густини
HOMO локалізовані на карбоксильних і карбонільних групах рамноліпіду, кисневі
атоми яких є донорами електронів (рис. 12а). Електронна густина LUMO
локалізована на гідроксильних групах молекули (рис. 12б). Це означає, що ці групи
можуть приймати електрони з металічних атомів (алюміній, мідь) з утворенням
антизв’язувальних орбіталей та працювати як акцептор електронів.
а б
Рис. 12. Розраховані енергії молекулярних орбіталей HOMO (а) та LUMO (б)
для молекули рамноліпіду.
Однак отримане числове значення ширини енергетичної щілини рамноліпіду
значно вище (7,785 еВ), ніж, наприклад, відомих інгібіторів, які містять аміногрупи
(≈ 3…4 еВ). Це свідчить про низьку реакційну здатність молекули загалом, що
підтверджують розрахунки її параметрів жорсткості (3,89 еВ) та м’якості (0,26 еВ), а