Page 88 - 2
P. 88
87
з поміж усіх досліджених розчинів. Такий характер залежностей пов'язаний з
тим, що в даному розчині поряд з водневою протікає і киснева деполяризація,
швидкість якої є вищою, і на катодну реакцією відновлення водню припадає
значно менша частина кількості електрики, ніж у двох попередніх розчинах.
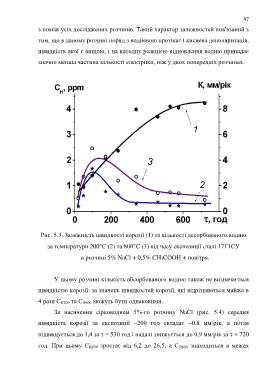
Рис. 5.3. Залежність швидкості корозії (1) та кількості десорбованого водню
за температури 200С (2) та 800С (3) від часу експозиції сталі 17Г1СУ
в розчині 5% NaCl + 0,5% CH 3COOH + повітря.
У цьому розчині кількість абсорбованого водню також не визначається
швидкістю корозії: за значень швидкостей корозії, які відрізняються майже в
4 рази С Н200 та С Н800 можуть бути однаковими.
За насичення сірководнем 5%-го розчину NaCl (рис. 5.4) середня
швидкість корозії за експозиції ~200 год складає ~0,8 мм/рік, а потім
підвищується до 1,4 за = 530 год і надалі знижується до 0,9 мм/рік за = 720
год. При цьому С Н200 зростає від 6,2 до 26,5, а С Н800 знаходиться в межах